第3種冷凍機械責任者、7900円
5.計画、8月9月は「初めての第3種冷凍機械責任者試験」の参考書を学習。
10月は「すぐわかる第3種冷凍機械責任者試験」の問題集を学習。
試験勉強にてわからないところ
p-h線図の見方がわからない。
日本冷凍空調学会にセミナー/継続学習/e-learningに冷凍サイクルの説明あり。
ここのp-h線図の冷凍サイクルの説明がわかりやすかった。
http://www.jsrae.or.jp/E-learning/saikuru/saikuru.html
| 2. | p-h線図上に冷凍サイクルを書く方法 |
(問題)
| 次の冷凍サイクルをp-h線図に書き込みなさい。 |
| (解答の手順) |
| (1) 凝縮器の線を引く |
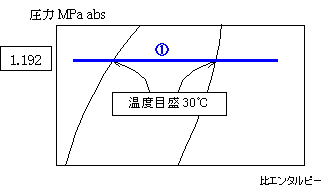
| 飽和蒸気線、飽和液線の30℃目盛りを通る水平線①を引きます。線の長さは後で直します。短かめの方が直すのに楽です。 |
| 30℃の凝縮圧力1.192MPa absを通る水平線でも同じです。 |
| (2) 蒸発器の線を引く |
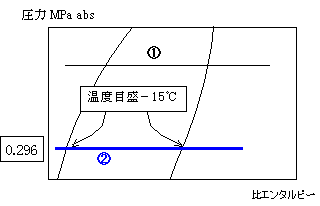
| 飽和蒸気線、飽和液線の-15℃目盛りを通る水平線②を引きます。 同様に、線の長さは後で直します。 |
| -15℃の蒸発圧力0.296MPa absを 通る水平線でも同じです。 |
| (3) 圧縮機の線を引く |
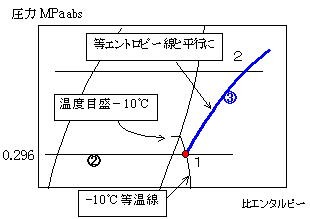
| 蒸発器の線②と-10℃等温線との交点(点1)は圧縮機吸込ガスの状態を示します。 点1から等エントロピー線と平行に曲線③を引きます。等エントロピー線は曲線です。 |
| (4) 膨張弁の線を引く |
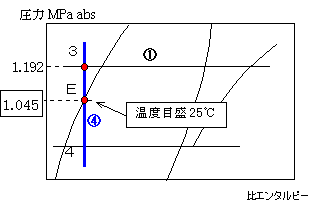
| 膨張弁前は25℃の過冷却液だから、ここでは、飽和液線の25℃(点E)を通る垂直線④を引きます。 線④と線①の交点3は膨張弁前の状態を示します。 |
| 25℃の飽和圧力1.045MPa absから 点Eを求めても同じです。 |
| (5) 図を仕上げる |
| 以上で冷凍サイクルをp-h線図に書き込むことが出来たが、このままでは見にくいので、点1~4より外の余分な線を消して下図の様に仕上げます。 線図より色々な値を読取ることができます。 |
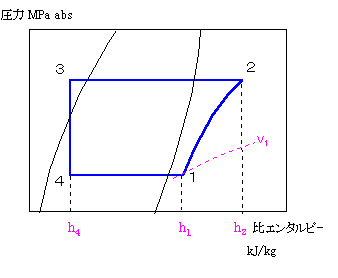
| 冷凍サイクルをうまくp-h線図に書き込めましたか。 この図から比体積(v1)と比エンタルピー(h1、h2、h4)が読み取れます。 |
| (解答) 各点の比体積、比エンタルピ-等は、 | |
| 比体積 | v1=0.08 m3/kg、 |
| 比エンタルピ- | h1=403 kJ/kg、 h2=438 kJ/kg、 h4=230 kJ/kg |
つまり冷凍サイクルを図示すると
p-h線図の逆台形の各頂点を1,2,3,4,とする。
p-h線図と飽和液線との交点をC,E, 飽和蒸気線との交点をA,Bとする。
またp-h線図の線分にある装置を()書きで示すと、(冷凍装置)をCCWで冷媒が流れる。
3--C---(凝縮器)---B------2
| <- /
E /
(膨張弁) ↓ ↑ (圧縮機)
| /
| -> /
4-----(蒸発器)----A--1
わかりにくい用語の説明
(1)比エンタルピーと、エンタルピーの違い
1kgの冷媒(物質)が持っているエンタルピーを比エンタルピーと言います。
比エンタルピーの単位は(kJ/kg)で、エンタルピーの単位は(kJ)です。
比体積(m3/kg)と体積(m3)との関係を思いだせばすぐ解りますね。
比エントロピーも同様です。
分りきったこととして、「比」を取ってしまうことも多いので注意してください。
(2)熱量とエンタルピーの違い
熱量とはある物質から外部へ放出した(または外部から取込んだ)熱エネルギーのことです。
エンタルピーはある物質が持っているエネルギー(熱+圧力Energy)です。
ある物質のエンタルピーが変化すると、その分だけ外部と熱や動力を出し入れします。
(これが熱力学の第1法則です。エネルギー保存の法則とも言います)
例えば、水1kgの温度が1℃下がるのは、4.186kJの熱量で冷却されたからです。
(4.186は水の比熱と言い、単位はkJ/(kg・K)です。昔の単位で1 kcal/kg℃)
(3)状態量とエネルギーの関係
圧力、温度、体積のようにある物質の状態を表すものを状態量と言います。
この他にエンタルピー、エントロピー、内部エネルギーなど色々な状態量があります。
状態変化によって発生するもの、例えば熱量、動力、仕事 等は状態量ではありません。
これらは物質が外部と出し入れするエネルギーです(外部エネルギーとも言います)。
(2)の例で、4.186kJの熱量は外部エネルギーです。
一方、1℃当り4.186kJ/kgだけ比エンタルピー(or内部エネルギー)が高いと言えば、
状態量としての記述です。
(4)エントロピー
熱は高温から低温の物質に流れ、逆には流れません。 (熱力学の第2法則)
(エントロピーは熱力学第2法則から導かれ、ds=dq/Tで示される状態量です。)
エントロピーとは、ある変化が可逆変化とどの程度違うかを示すものです。
可逆変化とは、外部とのエネルギーの出入りが逆転すると元に戻る変化です。
例えば、断熱圧縮のコンプレッサーを冷媒で駆動すると原理的には断熱膨張エンジンになります。
この様なものが可逆変化です。可逆変化ならばエントロピーは変化しません。
なお、断熱変化は必ずしも可逆変化ではありません。
冷凍サイクルでエントロピーを意識するのは圧縮工程です。
理想の圧縮工程では、冷媒とシリンダとの間に熱の出入りの無い断熱圧縮をし、
エントロピー変化もゼロです。だからP-h線図ではエントロピー線に沿ってコンプレッサーを書きます。
(注意) 膨張弁は断熱変化ですが可逆変化ではありません。
物質は高圧から低圧に流れ、逆には流れない からです。・・・これも第2法則の別表現
膨張、蒸発の行程は全て不可逆変化で、エントロピーは増加します。
(例題2) 下記の条件で運転している実際の冷凍サイクルをp-h線図に書込みなさい。
| 記号 | 場 所 | 圧 力 | 温 度 |
| ① | 圧縮機吸込み口 | 0.25 MPa | -4.5 ℃ |
| ② | 圧縮機吐出し口 | 1.90 MPa | 120 ℃ |
| ③ | 膨張弁前 | 1.80 MPa | 44 ℃ |
| ④ | 蒸発器入口 | 0.30 MPa | ― |
| ⑤ | 蒸発器出口 | 0.27 MPa | -10 ℃ |
(問題2 解答例) 実線が実際の冷凍サイクル、破線は理論冷凍サイクルです。




0 件のコメント:
コメントを投稿